
Valichi chiusi, aiuti bloccati. Israele avanza su Rafah
9 Maggio 2024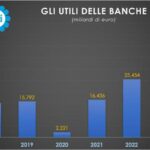
Banche, l’utile del trimestre cresce del 26% a 6,36 miliardi
9 Maggio 2024La battaglia contro il virus
Il vaccino anti Covid-19 di AstraZeneca non è più commercializzato nell’Unione Europea, e presto sarà ritirato in tutto il mondo. A prendere questa decisione è stata la stessa azienda produttrice di Vaxzevria, la multinazionale anglo-svedese con sede principale in Inghilterra, a Cambridge.
La scelta è stata motivata da AstraZeneca con «ragioni commerciali ». Infatti il vaccino (che fu il primo a essere sviluppato nel 2020 in collaborazione con l’università di Oxford), risulta ormai obsoleto, segnala l’azienda, e sono disponibili altri prodotti aggiornati alle ultime sottovarianti di Omicron. Pertanto «non c’è più stata domanda per il vaccino Vaxzevria, che di conseguenza non è stato più prodotto né distribuito».
Poiché non prevede ulteriori richieste del vaccino, AstraZeneca ha deciso di ritirarne l’autorizzazione all’immissione in commercio (Aic) lo scorso 5 marzo a Bruxelles per l’Europa e procederà in modo analogo presso le altre autorità regolatorie nel mondo, dove è stato utilizzato. Non negli Stati Uniti dove invece Vaxzevria non è stato mai autorizzato dalla Food and Drug Administration (Fda).
Vaxzevria è un vaccino a vettore virale (è utilizzato l’adenovirus degli scimpanzè per trasportare nelle cellule una porzione della proteina Spike del Sars-CoV-2), che viene somministrato in due dosi, ed è indicato per i soggetti dai 18 anni in su.
Tra le complicanze indicate come molto rare (un caso su 10mila) dalla Agenzia europea dei medicinali (Ema) nel foglietto illustrativo al momento di autorizzarne l’utilizzo – il 29 gennaio 2021 – figurano la trombosi trombocitopenica (Tts), caratterizzata da coaguli di sangue e bassi livelli ematici di piastrine e la sindrome di Guillain-Barré (un disturbo neurologico in cui il sistema immunitario danneggia le cellule nervose).
Proprio la possibilità che Vaxzevria «in casi molto rari» possa aver causato la trombosi trombocitopenica è stato ammesso da Astra-Zeneca a fine aprile, davanti all’autorità giudiziaria del Regno Unito. Infatti 51 famiglie hanno avviato una class action per i danni fisici subiti, dopo l’inoculo di
Vaxzevria, e che esse imputano al vaccino. Nonostante le dichiarazioni della multinazionale (che peraltro ribadiva che il suo vaccino ha un profilo di sicurezza accettabile, e che i benefici superano i rischi di effetti collaterali non voluti), le famiglie hanno rinunciato alla causa, perché i loro avvocati hanno suggerito che esiste la concreta possibilità che il ricorso venga respinto.
Negli Stati Uniti, invece, il vaccino antivirale di AstraZeneca non è mai stato introdotto. Infatti, nel marzo 2021 il Consiglio di monitoraggio dati e sicurezza (Data and safety monitoring board, Dsmb) degli Istituti nazionali della salute (Nih) avvisava sia l’azienda produttrice sia l’Autorità di ricerca e sviluppo avanzati per la biomedicina (Biomedical Advanced Research and Development Authority) sia l’Istituto nazionale per le allergie e le ma-lattie infettive (National Institute of Allergy and Infectious Diseases) che i dati delle sperimentazioni cliniche forniti da AstraZeneca erano «obsoleti» e che potevano «fornire una visione incompleta dell’efficacia del vaccino ». L’azienda veniva invitata a comunicarne di più aggiornati e accurati, ma questi dati non vennero più forniti, e la Fda non autorizzò mai l’utilizzo di Vaxzevria negli Stati Uniti.
Nel nostro Paese il caso più noto e grave di reazione avversa dopo la somministrazione di Vaxzevria si è registrata nel giugno 2021. Una ragazza di 18 anni, Camilla Canepa, morì due settimane dopo essersi vaccinata contro il Covid- 19 durante un open day di AstraZeneca in Liguria.
Per quella vicenda è in corso un processo a Genova per il quale sono imputati cinque medici (quattro di loro per omicidio colposo, tutti per falso ideologico): i pubblici ministeri ritengono che la ragazza avrebbe potuto essere salvata, se fossero state seguite le linee guida che indicavano gli accertamenti necessari per una corretta diagnosi della rara complicanza. Subito dopo la morte di Camilla, il Comitato tecnicoscientifico (Cts) propose di riservare la somministrazione di Vaxzevria alle persone con più di 60 anni. Proprio ieri un genovese di 37 anni si è visto riconoscere un risarcimento per le gravi reazioni avverse subite dopo la somministrazione di Vaxzevria. Lo ha reso noto il Codacons che ha dato assistenza legale al cittadino ligure. Il vaccino Vaxzevria non è più da tempo utilizzato in Italia.
AstraZeneca, nel comunicarne il ritiro, ricorda che del suo vaccino sono state fornite 3 miliardi di dosi nel mondo e che, secondo alcune stime indipendenti, solo nel primo anno di utilizzo oltre 6,5 milioni di vite umane sarebbero state salvate grazie a Vaxzevria.
Ieri mattina, riferiva il sito Internet del quotidiano inglese Daily Telegraph, dopo l’annuncio del ritiro del prodotto le azioni di AstraZeneca hanno accresciuto il loro valore in Borsa per circa 3 miliardi di sterline.





